RETOUR AU SOMMAIRE
RETOUR AU SOMMAIRE
Face à la prolifération des méthodes d’estimation de la qualité des eaux courantes, nous avons voulu présenter ici quelques règles d’interprétation des données hydrobiologiques et dégager les avantages et les inconvénients des approches chimique et biologique afin de guider les enseignants dans le choix méthodologique le plus adéquat.
Les limites d’application de ce document sont de deux ordres :
les méthodes présentées concernent les eaux courantes (eaux lotiques) et leur application à des eaux à courant très lent ou nul (eaux lentiques) constitue, à notre avis, un abus qui se solde par une estimation de qualité sans rapport avec la réalité; d’autres méthodes spécifiques, moins nombreuses, existent pour les milieux lentiques;
les méthodes présentées concernent essentiellement les pollutions organiques; les pollutions minérales, plus complexes, semblent avoir peu d’influence sur les peuplements d’algues et peuvent avoir une toxicité directe, éliminant la plupart des organismes animaux qui ne peuvent donc plus servir d’indicateurs; il convient, ici aussi, de recourir à d’autres méthodes basées sur l’accumulation des éléments minéraux polluants par des végétaux ou des animaux (accumulation de métaux lourds, de radioéléments,… dans des bryophytes, des mollusques, des poissons,…) et non plus sur des modifications de la composition des peuplements.
| retour
en haut de page |
1. LA POLLUTION ORGANIQUE ET SES CONSEQUENCES
Il convient tout d’abord de rappeler ce qu’est la pollution organique et ce qu’elle devient une fois rejetée dans la rivière sans transiter dans une station d’épuration.
En fait, les eaux résiduaires urbaines rassemblent les eaux grises (cuisine, bains) et les eaux noires (WC). Sel (NaCl), détergents, savons, urines et fèces constituent l’essentiel de leur contenu.
On peut définir la charge polluante journalière d’un habitant (soit l’équivalent-habitant ou EH) comme suit :
Charge hydraulique : 180 litres/j.hab
Charge en matières en suspension : 86 g/j.hab
Charge en DCO : 135 g-O2/j.hab
Charge en DBO5 : 54 g-O2/j.hab
Charge en azote total : 15 g-N/j.hab
Charge en azote Kjeldhal : 9 g-N/j.hab
Charge en phosphore total : 4 g-P/j.hab
Une partie des matières en suspension (matières organiques particulaires) va passer sous forme dissoute progressivement. On voit donc que le plus grande part des éléments polluants est sous forme organique. D’autre part, elle est surtout composée de carbone, d’azote et de phosphore.
Dès leur arrivée dans le réseau d’égouttage puis dans la rivière, ces matières organiques vont être transformées en matières minérales par l’action bactérienne en aérobiose (oxydation) puis en anaérobiose (fermentation) si la réoxygénation naturelle du cours d’eau n’est pas suffisante. Au bout de cette transformation, il reste du gaz carbonique émis dans l’atmosphère (et en partie dissous dans l’eau), des nitrates et des phosphates.
Le schéma ci-dessous, essentiel pour comprendre la suite du document, montre ce mécanisme de transformation qui est appelé " autoépuration des cours d’eau " et, brièvement, l’impact sur la faune et la flore qui sera détaillé plus loin. Le code de couleurs est maintenant utilisé partout : rouge pour la pollution organique très forte, l’orange pour la pollution organique forte, jaune pour l’eutrophisation, le vert pour la pollution faible (due à un peu d’organique ou à une eutrophisation faible) et le bleu pour les eaux naturelles.

|
Traces de C, N, P organiques Peu de nitrates Traces de phosphates Peu de bactéries fécales |
Beaucoup de C, N, P organiques Peu de nitrates Teneur modérée en phosphates Beaucoup de bactéries fécales |
Traces de C, N, P organiques Beaucoup de nitrates et de phosphates Diminution progressive de bactéries fécales |
Retour progressif à l'état naturel |
|
|
|||
|
NATUREL
|
POLLUE |
EUTROPHISE |
NATUREL |
|
P-PO4 : 0-15m g-P/l |
En rouge : zone très fortement altérée par la pollution organique
En orange : zone fortement altérée par la pollution organique |
En jaune : zone modérément altérée par une eutrophisation plus ou moins forte En vert : zone faiblement altérée par l'eutrophisation résiduelle |
P-PO4 : 0-15m g-P/l |
|
Flore et faune variée en équilibre, biomasse limitée, saturation en oxygène |
Elimination de toutes les espèces sensibles, développement de nombreuses bactéries filamenteuses (Sphaerotilus), restent quelques invertébrés et des algues diatomées très résistantes. Très peu ou pas d'oxygène. |
En zone jaune, prolifération des végétaux à cause des teneurs importantes en phosphates et nitrates, augmentation de la biodiversité par réapparition d'espèces sensibles. Beaucoup d'oxygène le jour, très peu la nuit (mortalité de poissons par asphyxie) |
Flore et faune variée, en équilibre, biomasse limitée, saturation en oxygène |
| retour
en haut de page |
On réalise, le plus généralement, un prélèvement momentané répété à des fréquences diverses (annuelle, saisonnière, mensuelle, journalière, horaire). Les éléments retenus pour le calcul des indices présentés ici sont l’oxygène dissous, la DCO, la DBO5, l’ammoniaque, les nitrites, les nitrates, le phosphore (orthophosphates et phosphore total), l’oxydabilité.
| retour
en haut de page |
Les analyses chimiques restent le seul moyen d’identifier la nature exacte des polluants et les teneurs qu’ils peuvent atteindre, notamment les teneurs maximales importantes pour leur effet direct plus particulièrement sur la faune.
Le prélèvement est simple et rapide et demande peu de matériel.
| retour
en haut de page |
Les analyses chimiques sont généralement momentanées. Vu les importantes fluctuations journalières et horaires des charges polluantes, un prélèvement momentané ou à une fréquence faible est très peu fiable et il est même téméraire d’effectuer une cartographie ou une surveillance de la qualité des eaux sur cette seule base aléatoire.
On peut pallier cet inconvénient en augmentant la fréquence des prélèvements suivant les buts poursuivis et les types de milieux ou en utilisant des échantillonneurs automatiques, ces deux solutions entraînant une forte augmentation du coût.
| retour
en haut de page |
2.1.4. Evaluation de la pollution organique : présentation de trois indices
Nous présentons ci-après 3 méthodes que l’enseignant pourra aisément appliquer à partir de ses propres analyses ou d’analyses venant de travaux publiés :
Indice de pollution organique (IPO, LECLERCQ & MAQUET, 1987)
Lisec-Index (BECKERS & STEEGMANS, 1979)
Classification des paramètres par l’Institut d’Hygiène et d’Epidémiologie (IHE, 1986)
Elles comportent toutes cinq classes de qualité correspondant aux couleurs généralement admises :

| retour
en haut de page |
A. INDICE DE POLLUTION ORGANIQUE (IPO, LECLERCQ & MAQUET, 1987)
La première est l’indice de pollution organique (IPO) mise au point à partir de plus de 1000 analyses chimiques et biologiques (algues diatomées). Le principe est de répartir les valeurs des éléments polluants en 5 classes, puis de déterminer, à partir de ses propres mesures, le numéro de classe correspondant pour chaque paramètre puis d’en faire la moyenne. Comme l’analyse de DOB5 nécessite un appareillage assez coûteux, les données ne sont pas souvent disponibles en rivières. On calcule alors la moyenne des numéros de classe avec les trois autres éléments.
Remarque : le seul paramètre en relation directe avec la pollution organique est la DBO5 mais on peut considérer que les autres, qui sont des formes déjà minérales, résultent directement de la minéralisation des matières organiques et reflètent bien ce type de pollution. Ils sont d’ailleurs en quantité toujours très faible dans les milieux naturels. L’idéal serait de remplacer l’ammonium et les nitrites par l’azote Kjeldahl et les phosphates par le phosphore total mais on dispose rarement de ces paramètres très coûteux.
|
Paramètres Classes |
DBO 5 mg–02/l |
mg –N/l |
nitrites µg-N/l |
phosphates µg-P/l |
|
5 4 3 2 1 |
< 2 2 – 5 5.1 – 10 10.1 – 15 > 15 |
< 0.1 0,1– 0.9 – 2.4 2.5 – 6.0 > 6 |
5 6 – 10 11 – 50 51 – 150 > 150 |
15 16 – 75 76 – 250 251 – 900 > 900 |
IPO = moyenne des numéros de classes des 4 paramètres (au mieux) :
= 5.0 – 4.6 : pollution organique nulle
= 4.5 – 4.0 : pollution organique faible
= 3.9 – 3.0 : pollution organique modérée
= 2.9 – 2.0 : pollution organique
= 1.9 – 1.0 : pollution organique très forte
Si l’analyse a donné les résultats suivants :
DBO5 : 7 mg-O2/l classe 3
Ammonium : 0,8 mg-N /l classe 4
Nitrites : 75 µg-N/l classe 2
Phosphates : 265 µg-P/l classe 2
IPO = 3 + 4 + 2 + 2 /4 = 2,8 :
Si on n’a pas la mesure de DBO5, IPO = 2,7 : pollution organique forte
| retour
en haut de page |
B. LISEC-INDEX (BECKERS & STEEGMANS, 1979)
Le principe est le même que celui de l’IPO mais on calcule la somme des valeurs de classe et non la moyenne. ATTENTION : les classes sont numérotées en sens inverse de celles de l’IPO : ainsi, un indice élevé correspondra à une pollution importante.
|
N° de classe |
Oxygène dissous % de saturation |
DBO5 mg-O2/l |
Ammonium mg-N/l |
Phosphore total m g-P/l |
|
1 2 3 4 5 |
91-110 71-90 51-70 31-50 £ 30 |
3 3,1-6,0 6,1-9,0 9,1-15,0 >15 |
< 0,5 0,5-1,0 1,1-2,0 2,1-5,0 > 5 |
50 51-249 250-899 900-1499 ³ 1500 |
|
LISEC-INDEX = somme des numéros de classe : 4 - < 6 : très bon 6 - < 10 : bon 10 - < 14 : moyen 14 - < 18 : 18 – 20 : très mauvais |
||||
Si l’analyse a donné les résultats suivants :
DBO5 : 7 mg-O2/l classe 3
Ammonium : 0,8 mg-N /l classe 4
Nitrites : 75 µg-N/l
Phosphates : 265 µg-P/l
On obtient un Lisec-Index de (3 + 4) x 2 (deux paramètres sur quatre disponibles) soit 14 ou qualité moyenne.
Remarque : il convient de toujours remplacer le mot " pollution moyenne " par " pollution modérée ", le premier faisant croire qu’on pourrait avoir calculé une moyenne à partir de plusieurs analyses.
| retour
en haut de page |
C. CLASSIFICATION DES PARAMETRES (INSTITUT D’HYGIENE ET D’EPIDEMIOLOGIE, 1986)
C’est la même méthode que l’IPO (répartition des valeurs en 5 classes) mais il s’agit d’autres paramètres et d’autres classes.
|
Paramètres/ classes |
Oxygène dissous % |
D.C.O mg-O2/l |
B.O.D.5 mg-O2/l |
Ammonium mg-N/l |
Phosphates m g-P /l |
Phosphore total m g-P /l |
|
5 4 3 2 1 |
90-110 70-89 50-69 30-49 <30 |
£ 5,0 5,1-10,0 10,1-20,0 20,1-50,0 >50,0 |
£ 1,0 1,1-3,0 3,1-5,0 5,1-10,0 >10,0 |
£ 0,05 0,06-0,50 0,51-1,00 1,01-2,00 >2,00 |
£ 50 51-100 101-200 201-400 >400 |
£ 50 51-100 101-200 201-400 >400 |
|
*selon Min. de la Santé publique et de la famille, Inst. D’Hygiène et d’Epidémiologie, sept. 1986. (des classes sont aussi définies pour la dureté totale, la conductivité, les chlorures, les sulfates, les fluorures, le mercure, le cadmium, le chrome, le plomb, les cyanures totaux, les détergents anioniques, les détergents anioniques et les hydrocarbures polyaromatiques). |
||||||
L’IHE ne prévoyait pas de calculer un indice mais utilisait ces classes pour établir des cartes de qualité par paramètre.
Pour obtenir une note synthétique, nous appliquons à ce tableau le mode de calcul de l’IPO et sa clé d’interprétation :
5.0 – 4.6 : pollution organique nulle
4.5 – 4.0 : pollution organique faible
3.9 – 3.0 : pollution organique modérée
2.9 – 2.0 : pollution organique
1.9 – 1.0 : pollution organique très forte
Si l’analyse a donné les résultats suivants :
DBO5 : 7 mg-O2/l classe 2
Ammonium : 0,8 mg-N /l classe 3
Nitrites : 75 µg-N/l
Phosphates : 265 µg-P/l classe 2
On obtient un indice de (2 + 3 + 2) / 3 soit 2,3 ou
| retour
en haut de page |
Calculer les trois indices à partir du tableau de mesure ci-dessous.
Il résulte d’une étude d’un cours d’eau belge, la Joncquière, examiné en 6 points disposés de l’amont vers l’aval :
premier point en amont du village de Doische (700 habitants) qui rejette toutes ses eaux usées directement dans la rivière (la station d’épuration fut mise en service un an après l’étude),
le deuxième point en aval du rejet,
les trois suivants en parcours forestier sans nouveaux apports polluants,
le sixième en aval de Vaucelles, petit village sans station d’épuration.
Attention : le budget de cette étude a permis de faire une campagne d’analyse par mois et donc de présenter ici des moyennes annuelles. Il ne s’agit donc pas de mesures momentanées.
|
LIEU DE PRELEVEMENT |
Oxygène en % |
DCO mg-O2/l
|
DBO5 mg-O2/l |
ammonium mg – N/l |
nitrites µg – N/l |
phosphates µg-P/l |
nitrates mg-N/l |
|
|
1 2 3 4 5 6 |
amont du village aval du rejet 1,5 km en aval du rejet 3 km en aval du rejet 4,5 km en aval du rejet 5,5 km en aval du rejet et en aval de Vaucelles |
95 66 74 93 100 89 |
28.3 151.1 91.3 63.1 37.0 63.4 |
2.1 7.8 6.2 4.4 3.6 4.3 |
0.2 1.7 1.5 0.5 0.2 0.4 |
4 43 59 58 35 53 |
35 470 380 325 215 155 |
0.8 1.9 1.9 2.5 4.6 4.6 |
Pour bien comparer les résultats des trois méthodes, il conviendrait de calculer les indices à partir d’un même tableau de données. On se heurte directement à une difficulté : les paramètres utilisés sont différents pour chaque indice, deux seulement étant communs (DBO5 et ammonium). D’autre part, on est contraint de calculer les indices incomplètement à partir des paramètres dont on dispose. Les indices sont donc difficiles à comparer.
L’interprétation est aussi difficile puisque les limites de classe sont différentes suivant les méthodes : par exemple, pour les phosphates, la valeur limite des eaux naturelles est de 15 µg-P/l pour l’IPO, de 50 µg-P/l pour l’IHE, même de 100 µg-P/l pour un autre indice non considéré ici.
En dépit de ces difficultés, la grille de comparaison des indices nous permet de dégager quelques tendances. La figure 1 donne le profil amont-aval des valeurs indicielles pour les stations de la Joncquière : afin de travailler sur une même échelle (entre 1 et 5), une transformation mathématique est appliquée au Lisec-Index.
|
LISEC-INDEX * |
IHE |
IPO |
||||
|
indice |
classe |
indice |
classe |
indice |
classe |
|
|
1 2 3 4 5 6 |
4 12 10,6 6,7 5,3 6,7 |
nulle modérée modérée faible nulle faible |
4.0 1.8 2.2 3.0 3.2 3.0 |
faible très forte modérée modérée modérée |
4.3 2.8 2.5 3.0 3.5 3.3 |
faible
modérée modérée modérée |
Calculé sur 3 paramètres au lieu de 4 ! Les valeurs du tableau sont alors obtenues en multipliant la cote par 1,33 (rapport entre 20 et 15) pour les ramener sur un maximum de 20.
La figure 1 montre que les profils amont-aval sont généralement parallèles : les indices reflètent tous la brusque dégradation en aval du village (station 2) puis l’autoépuration progressive en parcours forestier (stations 3, 4 et 5) et enfin une nouvelle altération en aval du village de Vaucelles (station 6). Attention : ne pas oublier que l’échelle du Lisec-Index va en sens inverse et jusqu’à 20
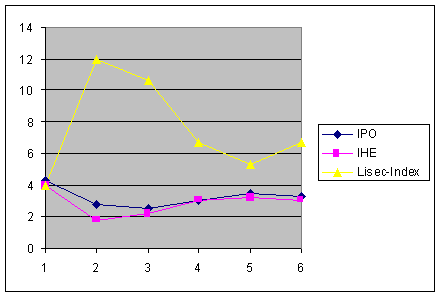
Figure 1. – Comparaison des 3 indices de pollution dans les 6 stations de la Joncquière, calculés à partir des moyennes annuelles des paramètres.
Par contre, la comparaison des classes de pollution est beaucoup moins satisfaisante, de grands écarts étant observés. Les plus importants sont notés à la station 2 où la pollution est la plus forte et la plus évidente : pollution modérée pour le Lisec-Index, très forte pour l’IHE, forte pour l’IPO.
Nous l’avons dit, ces divergences proviennent du choix des paramètres et des classes. Dans le cas présent, on peut certifier que le Lisec-Index est trop optimiste : pollution modérée là où elle est la plus marquée ce qui s’observe aisément sur le terrain : bactéries, odeurs ; pollution faible (station 4 et 6) quand on a 325 et 155 µg-P/l en phosphates. Les deux autres indices sont assez proches et plus réalistes : ils repèrent bien la pollution la plus forte et l’altération par les phosphates qui annoncent l’eutrophisation.
| retour
en haut de page |
2.1.5. Evaluation de l’eutrophisation
Il n’y a aucun indice fiable pour évaluer le niveau d’eutrophisation à partir de la chimie. Comme ce phénomène est clairement lié à un excès de nutriments minéraux provenant soit directement de l’agriculture (engrais), soit de la minéralisation de la matière organique des eaux usées, on a tenté de mettre au point certains indices sur base des teneurs en nitrates et en phosphates. Toutefois, des expériences de pollutions artificielles ont montré que les nitrates seuls n’entraînent pas une augmentation importante de la production végétale alors qu’un faible apport de phosphates suffit à déclencher la prolifération végétale. Il est donc bien connu que c’est le phosphore qui est l’élément limitant. Comme il est très coûteux de l’éliminer des eaux usées, le problème de l’eutrophisation subsistera encore longtemps.
Finalement, nous suggérons une interprétation très simple : quand la teneur dépasse 15 µg-P/l, il y a début d’eutrophisation. Pour mieux en connaître l’ampleur, la simple analyse des phosphates ne suffira pas car la part de cet élément mobilisée dans les végétaux échappe à l’analyse. Il faudra donc obligatoirement utiliser des méthodes biologiques c’est-à-dire évaluer le niveau d’eutrophisation via l’effet des phosphates sur la biocénose végétale (études de productivité primaire), en n’oubliant pas d’étudier aussi des stations naturelles pour établir un système de référence pour chaque bassin versant, les différents types d’eau (oligotrophe, mésotrophe, eutrophe) ayant une productivité propre.
| retour
en haut de page |
Il apparaît que les trois méthodes proposées font bien ressortir le phénomène de pollution organique suivi par l’autoépuration et il est même possible de mettre en évidence des modifications assez faibles dues par exemple au rejet de quelques habitations seulement mais à condition de travailler sur des moyennes calculées sur un nombre suffisant d’analyses.
La difficulté est de déterminer, à partir des indices, les niveaux de pollution car chaque indice a sa clé d’interprétation, souvent établie de façon subjective.
A notre connaissance, seul l’indice IPO fait intervenir les paramètres strictement liés aux pollutions organiques : on écarte la DCO (mesurable aussi en milieux naturels quand on a des acides humiques) et l'oxygène (présent dans des eaux très polluées pourvu qu'elles soient bien agitées ou très riches en végétaux et par contre en déficit permanent dans les sources naturelles).
Certains pourraient être étonnés de ne pas voir figurer les nitrates. Il faut savoir que, dans les milieux naturels, on a un niveau de base en nitrates variable suivant le niveau trophique de la rivière (donc plus faible en eau olitrophe qu’en eau eutrophe) mais qui n’est pas bien connu. Il faudrait donc tenir compte seulement de la différence entre la mesure et la valeur naturelle supposée pour évaluer correctement la contamination.
Le même commentaire s'applique à la DCO influencée par des éléments naturels (matières en suspensions, acides humiques).
Il n’en est pas de même pour les phosphates qui sont en quantité très faible (inférieure à 15 µg-P/l) dans les milieux naturels de tous niveaux trophiques et qui, indirectement, peuvent servir d’indicateurs de pollution organique.
Les phosphates jouent un rôle capital dans le fonctionnement de l’écosystème, étant à la base de la production des végétaux aquatiques qui serviront de nourriture aux animaux. La chimie ne permet pas de fixer correctement le niveau d’enrichissement en cet élément car il est généralement absorbé par les plantes pendant les périodes de végétation. Quand ces plantes meurent pendant la mauvaise saison, le phosphore est relargué mais de façon progressive et dilué par les hautes eaux. L’évaluation de niveau d’eutrophisation, phénomène très dommageable pour la faune piscicole, revêt une grande importance économique et ne peut se faire correctement qu’en utilisant les bio-indicateurs adéquats (voir plus loin l’étude de la productivité primaire et des diatomées).
| retour
en haut de page |
2.2. LES METHODES BACTERIOLOGIQUES
2.2.1. Le monde bactérien des eaux douces
Outre les organismes végétaux et animaux aquatiques habituels, une foule de micro-organismes peuple les eaux de façon normale ou non. Certains peuvent devenir une gêne pour l'environnement ou pour l'homme. Ainsi, certains génèrent des composés difficiles à éliminer qui communiquent à l'eau un goût de terre, de vase, de moisi (mycobactéries actinomycètes). D'autres peuvent attaquer les parois des conduites avec apparition d'eaux rouges et troubles (ferrobactéries). Enfin, certains peuvent porter atteinte à la santé humaine (micro-organismes pathogènes).
Les analyses bactériologiques de l'eau ont pour but :
de rechercher si les populations bactériennes naturelles de type " décomposeur " sont bien équilibrées de manière à assurer une bonne remise en circulation des éléments minéraux à partir des organismes morts;
de mettre en évidence la présence de bactéries qui indiquent une pollution fécale due à un rejet d’eaux résiduaires urbaines et (ou) qui modifient l’aptitude de l’eau à une utilisation donnée (eau potabilisable, eau de baignade, eau à utilisation industrielle,…).
Ce sont ces dernières que nous envisagerons ici, comme estimateur de la contamination fécale. Ainsi, en cas de risque de pollution par des eaux résiduaires, on recherchera les germes les plus classiques :
Bactéries d’habitat fécal normal et exclusif : Escherichia coli (+ les coliformes fécaux) et les streptocoques fécaux : leur présence dans une eau apporte la certitude d’une contamination fécale. C’est la seule indication fournie par une analyse isolée et il sera nécessaire de répéter l’échantillonnage si l’on veut tenter une interprétation plus précise. L’interprétation est rendue complexe par :
la durée variable de survie de ces germes dans le milieu aqueux, assez limitée pour E. coli, plus élevée pour les coliformes et très longue pour les streptocoques fécaux;
les variations qualitatives des flores intestinales : 4 fois plus d’E. coli que de streptocoques fécaux chez l’homme, 6 fois moins chez la vache et 20 fois moins chez le porc dont les déjections ne contiennent pratiquement que des streptocoques fécaux : cette particularité peut-être mise à profit, avec précaution, pour identifier la source de pollution.
Bactéries d’habitat non exclusif : elles vivent aussi bien dans les matières fécales que dans le milieu extérieur : coliformes (autres que E. coli et coli fécaux), Clostridium sulfito-réducteurs.
Les bactériophages exclusivement fécaux apportent une preuve irréfutable d’une contamination et sont intéressants car ils subsistent dans le milieu récepteur plus longtemps que les bactéries fécales et, en raison de leur taille plus petite, semblable à celle des virus, ils peuvent percoler vers les nappes et servir alors d’indicateurs de pollution virale fécale à ce niveau.
On détermine également souvent le nombre de bactéries totales mais ce chiffre est extrêmement variable et très difficile à interpréter : il varie considérablement en fonction des pluies, sources d’une contamination météorique et par lessivage des sols avoisinants. Ce nombre ne permet évidemment pas de repérer une contamination fécale.
| retour
en haut de page |
2.2.2. Indice de qualité microbiologique (iqm) : principe
Comme pour les analyses chimiques, il est possible de calculer pour les cours d’eau un indice de contamination bactériologique à partir du dénombrement de différents germes dont les principaux, généralement associés à la pollution organique, sont les bactéries totales, les coliformes fécaux et les streptocoques fécaux.
Le prélèvement en flacon stérile de 500 ml est simple mais constitue un échantillon ponctuel et momentané qui, pour certaines études, ne sera guère représentatif. Il convient donc de déterminer la fréquence d’échantillonnage en fonction du but poursuivi, des conditions atmosphériques, des saisons… Dans certains cas (bords escarpés, ponts,…), il sera nécessaire de disposer d’une perche à l’extrémité de laquelle on fixe le flacon de prélèvement. L’échantillon doit être transporté en enceinte réfrigérée (boite frigo par exemple) et ensemencé le jour même.
Nous n’entrerons pas ici dans les détails de la mise en culture et du dénombrement qui seront généralement confiés à un laboratoire spécialisé.
Il existe cependant sur le marché des tests relativement simples présentés en kit et qui permettent une détection assez rapide des germes fécaux de manière qualitative (présence-absence) ou semi-quantitative (nombre le plus probable).
| retour
en haut de page |
Ce type d’analyse est extrêmement sensible, la moindre contamination qui échapperait à l’analyse chimique, étant mise en évidence. Comme pour les autres paramètres, il importe évidemment de connaître les niveaux naturels de référence.
Suivant les types de germes, il est possible d’identifier, dans une certaine mesure, la source de contamination fécale (humaine, bovine, porcine).
Le prélèvement est simple et rapide, nécessitant seulement des flacons stériles.
| retour
en haut de page |
Les niveaux de contamination sont très largement dépendants des débits, du lessivage des sols, du moment du prélèvement,… Un prélèvement ponctuel et unique a donc peu de signification. D’autre part, il n’y a pas d’effet intégrateur, les bactéries d’origine fécale étant au contraire condamnées à disparaître progressivement des rivières dont le régime thermique est incompatible avec leurs exigences.
L’investissement en appareillage et produits est assez important, compte tenu du caractère très momentané du renseignement fourni, et les analyses réalisées dans des laboratoires spécialisés sont coûteuses.
| retour
en haut de page |
2.2.5. Calcul de l’indice de qualité microbiologique (iqm)
Les limites des classes ont été établies par BOVESSE & DEPELCHIN (1980).
|
Classe n° |
Bact. tot./ml |
colif. f./ml |
strepto. f./ml |
|
5 4 3 2 1 |
<2000 2000-9000 9000-45000 45000-360000 >360000 |
<100 100-500 500-2500 2500-20000 >20000 |
<5 5-10 10-50 50-500 >500 |
Nous proposons le calcul de la moyenne des numéros de classes, comme pour l’IPO (chapitre 2.1.4.A.) et l’interprétation suivante :
|
IQM |
Contamination fécale |
|
4,3-5,0 3,5-4,2 2,7-3,4 1,9-2,6 1,0-1,8 |
nulle faible modérée très forte |
Ce système est appliqué au tableau de mesures suivant qui reprend des valeurs moyennes annuelles calculées à partir de prélèvements bimensuels.
|
Station n° |
LIEU DE PRELEVEMENT |
Bact. tot./ml |
colif. f./ml |
strepto. f./ml |
Indice |
contamination |
|
1 2 3 4 5 6 |
amont du village aval du rejet 1,5 km en aval du rejet 3 km en aval du rejet 4,5 km en aval du rejet 5,5 km en aval du rejet et en aval de Vaucelles |
28147 63941 50862 36356 24947 28122 |
65 1652 330 181 85 101 |
15 509 404 134 73 192 |
3.7 2.0 2.7 3.0 3.3 3.0 |
faible modérée modérée modérée modérée |
La contamination est faible en amont et forte en aval du village, puis diminue régulièrement. L’augmentation des germes, surtout les streptocoques, à la station 6 (aval de Vaucelles), correspond bien à de nouveaux rejets (quelques maisons, une ferme).

figure 2. – Evolution de la contamination fécale dans les 6 stations de la Joncquière, IQM calculés à partir des moyennes annuelles.
Sans donner ici le détail des comptages, signalons cependant que de très fortes différences existent entre les campagnes de prélèvement, surtout dans les stations polluées. A la station 3 par exemple, on compte 55 coliformes / ml le 7 mars 1988 (pollution nulle) et 8100 le 14 septembre 1987 (pollution forte). En conséquence, un seul prélèvement momentané ne suffit pas à établir un diagnostic fiable : il établit seulement la certitude de la contamination et non son importance.
| retour
en haut de page |
Comme pour les analyses chimiques, les analyses microbiologiques n’ont de signification que si on peut calculer des nombres moyens à partir d’un nombre suffisant de prélèvements (au moins 1 par mois), en se dégageant ainsi de différentes sources de variabilité (débit, jour et heure du prélèvement,…).
L’amélioration amont-aval ne résulte pas d’une auto-épuration mais d’une décontamination naturelle par mortalité des germes soumis à des conditions défavorables.
| retour
en haut de page |
Pour rappel, en sciences naturelles, on a mis au point une nomenclature hiérarchisée comprenant successivement :
- des embranchements,
- des classes,
- des ordres,
- des familles,
- des genres,
- des espèces.
A ce schéma classique peuvent s’ajouter des subdivisions (sous-embranchements,… et, au niveau infraspécifique, les sous-espèces, variétés, formes).
Chaque organisme reçoit donc un nom de genre et un nom d’espèce (par exemple Navicula atomus) éventuellement suivi d’un nom de sous-espèce, de variété,… (Navicula atomus var. permitis). Les noms latins sont écrits en italiques.
Au sein de chaque genre sont classées des espèces ayant des exigences écologiques différentes et, qui, en principe, doivent toutes apporter leur contribution dans le calcul d’un indice de qualité d’eau.
Deux types d’organismes benthiques (= vivant sur le fond de la rivière) ont surtout été utilisés jusqu’à présent pour le calcul d’indices de qualité : les diatomées (algues microscopiques) et les macro-invertébrés benthiques.
Au niveau des diatomées toutes groupées en une seule classe, la systématique a fait récemment de grands progrès et des ouvrages très complets avec de nouvelles clés d’identification et de nombreux documents photographiques sont maintenant disponibles. L’identification jusqu’au niveau de l’espèce et dans le cadre d’une nomenclature moderne étant possible, nous estimons que cette démarche est devenue obligatoire si l’on veut obtenir des indications fiables, même si elle demande une période de formation de quelques mois supervisée par un spécialiste. Toutefois, une clé des genres a été publiée : elle permet le calcul d’un " indice générique ", moins précis que " l’indice spécifique " mais pouvant donner satisfaction pour des démonstrations vulgarisées.
|

|
|||
|
|
|
 |
|
|
|
|||
Par contre, au niveau des macro-invertébrés benthiques, deux problèmes se posent :
la grande diversité d’organismes, appartenant à plusieurs embranchements pour lesquels les critères d’identification sont très différents, rend l’identification spécifique très difficile et demande l’utilisation d’une bibliographie très importante et dispersée ;
s’il est actuellement possible de déterminer la plupart des formes adultes jusqu’à l’espèce, il est par contre quasiment impossible d’identifier les larves aquatiques de certains groupes jusqu’à ce niveau.
|
Plécoptères |
Insectes 
Ephéméroptères |

Trichoptères |
|
|
Hémiptères
|
Coléoptères |
Diptères |
|
|
Crustacés
|
Mollusques
|
||
|
Vers segmentés
|
|||
|
Oligochètes |

Hirudinae
|
||
Dans l’état actuel des connaissances, établir un indice de qualité d’eau basé sur l’identification au niveau spécifique semble donc très difficile et prendrait un temps considérable. Signalons cependant qu’un tel indice existe (indice saprobique de SLADECEK, 1973), avec une liste impressionnante d’organismes dont les exigences écologiques sont précisées.
Pour les macro-invertébrés, on en est donc généralement réduit à simplifier considérablement le travail en fixant des niveaux aisés d’identification (famille, genre, quelquefois espèce) : la perte d’information qui en découle diminue la fiabilité et la sensibilité des indices.
| retour
en haut de page |
2.3.2. Les bio-indicateurs intégrateurs
Certains organismes enregistrent et intègrent toutes les modifications naturelles ou d'origine anthropique des facteurs abiotiques.
Pour être des bio-indicateurs valables, ces organismes doivent répondre à quelques critères importants.
Un groupe d’organismes sera intéressant si on peut trouver des espèces de ce groupe dans tous les milieux concernés, quel que soit le niveau de pollution.
La répartition des organismes choisis doit dépendre prioritairement des caractéristiques chimiques de l’eau si on veut estimer les niveaux de qualité.
Les organismes doivent être facilement identifiables à l’espèce afin d’être utilisés dans des méthodes de routine.
Des bio-indicateurs valables doivent présenter des exigences écologiques aussi étroites que possible, plus spécialement vis-à-vis des paramètres de la pollution organique.
Pour les organismes à large répartition, il serait intéressant d’arriver à une méthode applicable dans un large cadre géographique.
Nous verrons dans quelle mesure les diatomées et les macro-invertébrés répondent à ces différents critères.
| retour
en haut de page |
Les diatomées sont des algues microscopiques de couleur brun-jaune à l'état vivant, pourvues d'un squelette siliceux sur lequel est basée toute la systématique (fig. 3). Elles forment sur les pierres immergées des recouvrements homogènes brun-foncé gélatineux particulièrement visibles en hiver, en mai-juin et en septembre-octobre. On les trouve dans tous les types de milieux aquatiques, propres ou très pollués, sombres ou bien éclairés et quelques espèces peuvent vivre en milieu terrestre humide. Elles sont très sensibles aux contaminations azotées et phosphorées : à titre d'exemple, la composition des peuplements se modifie déjà sensiblement pour des teneurs de 30 m g-P/l.
L'observation des diatomées dans de bonnes conditions nécessite un nettoyage du prélèvement à l'acide nitrique qui élimine la matière organique du contenu cellulaire tout en sauvegardant le squelette siliceux.
Comme nous l'avons dit dans l'introduction, le calcul d'un indice fiable passe obligatoirement par l'identification jusqu'au niveau de l'espèce et par un comptage.
Contrairement aux analyses chimiques et bactériologiques dont les modes opératoires sont bien connus, nous décrirons en détail la procédure à suivre, depuis le prélèvement jusqu'au calcul de l'indice.
| retour
en haut de page |
Brosser la face supérieure des pierres immergées en courant rapide, sur une surface d'environ 200 cm2 (une ou plusieurs pierres suivant leur taille, brosse à gros poils de nylon).
Recueillir l'ensemble du prélèvement dans un flacon de 250 ml en rinçant la (les) pierres avec l'eau de la rivière.
Fixer avec 10 ml de formol à 10%, soit directement sur le terrain, soit dès le retour au laboratoire.
Remarque : en l'absence de pierres, 3 substrats artificiels peuvent être placés dans chaque station pendant environ 1 mois : l'expérience nous a montré que les systèmes les plus simples et les plus discrets donnaient de très bons résultats : nous en présentons un à la figure 3.
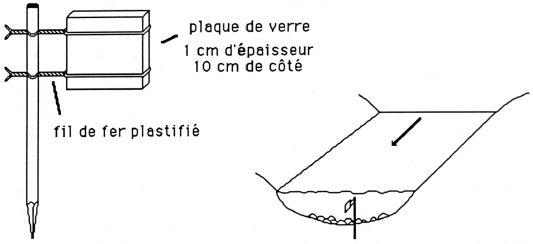
Figure 3. - Dispositif expérimental pour la récolte de diatomées en l'absence de substrat caillouteux naturel (également utilisable pour l'étude de la productivité primaire) D'après FABRI & LECLERCQ (1984).
| retour
en haut de page |
Laisser décanter pendant quelque jours ou, si le temps presse, centrifuger l'échantillon;
Eliminer le surnageant, verser le dépôt dans un berlin pyrex ajouter un même volume d'acide nitrique technique (40° Baumé) et laisser bouillir sous hotte, sur plaque chauffante jusqu'à élimination de toute la matière organique c'est-à-dire jusqu'à disparition du dégagement de vapeurs brunes d'acide nitreux. Si le volume de l'échantillon n'est pas trop important, une dizaine de minutes sont généralement nécessaires et suffisantes (procédure possible aussi avec de l’eau oxygénée, à chaud ou à froid).
Centrifuger pendant 10' à 3000 tours/min, éliminer le surnageant acide, rincer le culot à l'eau distillée et centrifuger à nouveau; répéter cette opération plusieurs fois si le surnageant est encore jaune.
Eliminer le dernier surnageant et remettre le culot en suspension dans de l'eau distillée ou de l'alcool, dans un petit flacon hermétique d'environ 20 ml.
| retour
en haut de page |
Homogénéiser l'échantillon nettoyé.
Prélever quelques gouttes de cette suspension et les déposer sur une lamelle couvre-objet ronde ou rectangulaire, d'épaisseur standard; laisser sécher sur plaque chauffante en veillant à avoir une répartition homogène du matériel; vérifier directement au microscope (objectif 20 x) si la densité de la préparation est convenable (au maximum une centaine de diatomées par champ microscopique avec l'objectif 20 x).
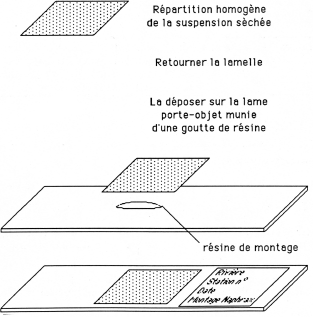
Figure 4. - Schéma de montage d'une préparation définitive de diatomées.
Si la densité convient, mettre 1 à 2 gouttes d'une résine de montage (Naphrax en solution dans le toluène), déposer dessus le couvre-objet et remettre sur plaque chauffante jusqu'à évaporation complète du toluène.
Retirer la préparation et la laisser refroidir en appuyant légèrement sur le couvre-objet : les bulles disparaissent et la préparation se solidifie rapidement (quelques secondes).
La préparation est définitive ; après étiquetage, elle peut être classée verticalement dans des coffrets.
| retour
en haut de page |
D. OBSERVATION ET COMPTAGE (figure 5).
Ces étapes se font obligatoirement avec des objectifs à immersion dans l'huile (indice de réfraction à 20° = 1,515), un 40x ou 50x ou 100x pour l'observation des structures fines.
Après identification des principales espèces, on réalise un comptage de toutes les espèces contenues dans une série de champs microscopiques pris au hasard, jusqu'à atteindre un total compté d'environ 500 individus. Les résultats sont ensuite exprimés en pourcentage d'abondance relative pour chaque espèce.
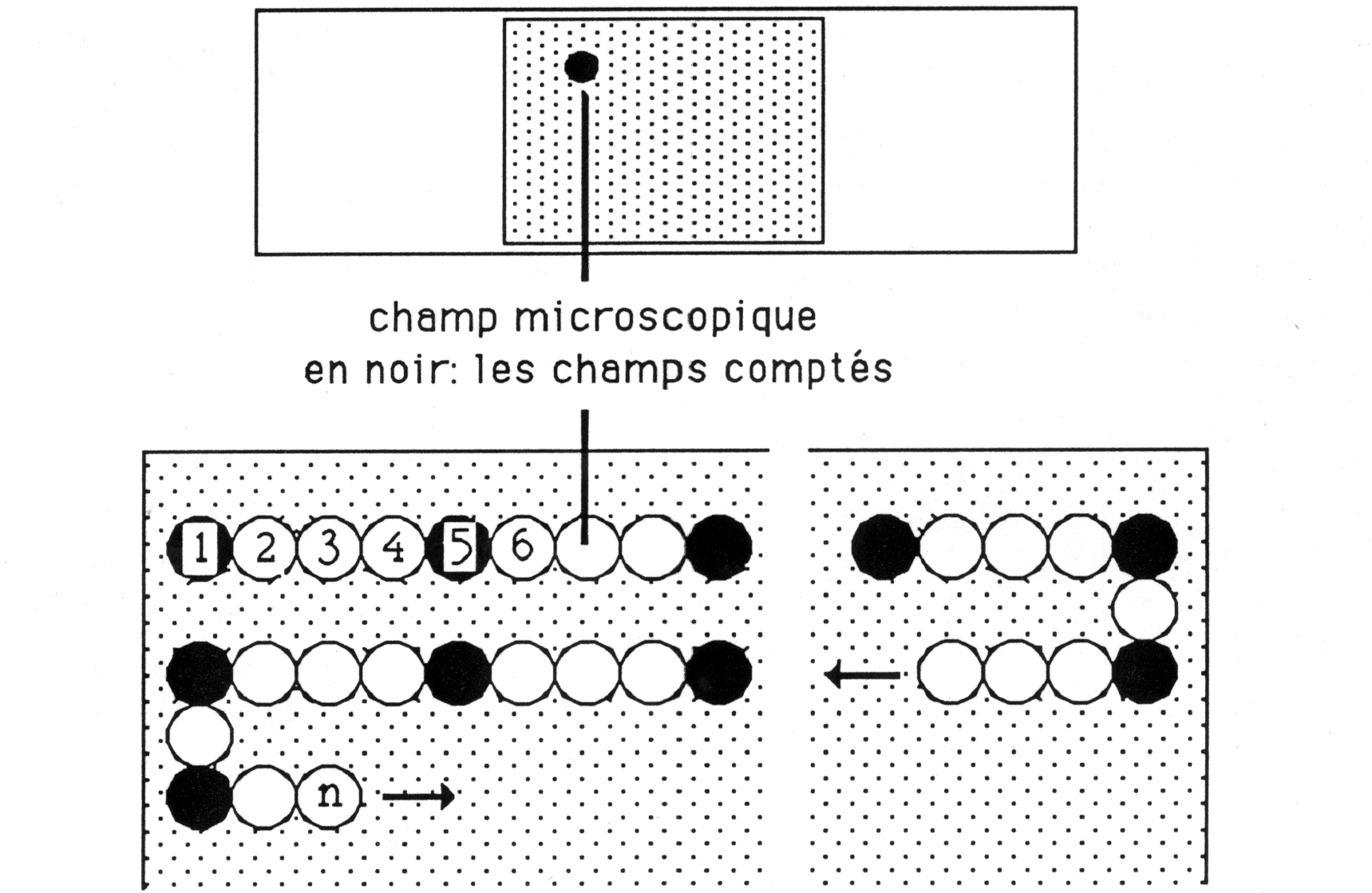
Figure 5. : Procédure et tableau de comptage
| retour
en haut de page |
Nous conseillons l'utilisation des ouvrages suivants :
- flores simplifiées d'identification des genres pour les débutants :
FABRI R., LECLERCQ L. & SWINNEN G., 1981. - L'étude des Diatomées : généralités et clé pratique des principaux genres observés en eau douce. Probio-Revue, 4 (1) : 23-42.
RUMEAU A. & COSTE M., 1988. - Initiation à la systématique des diatomées d'eau douce. Bull. Fr. Pêche Piscic., 309 : 1-69
- flores spécialisées avec identification des espèces :
GERMAIN H., 1981. - Flore des diatomées. Paris, Boubée, 444 p.
KRAMMER K. & LANGE-BERTALOT H., 1986. - Süsswasserflora von Mitteleuropa. Bacillariophyceae. 2/1: Naviculaceae. G. Fischer Verlag, Stuttgart, 876 p.
KRAMMER K. & LANGE-BERTALOT H., 1988. - Süsswasserflora von Mitteleuropa. Bacillariophyceae. 2/2: Bacillariaceae, Epithemiaceae, Surirellaceae. G. Fischer Verlag, Stuttgart, 596 p.
KRAMMER K. & LANGE-BERTALOT H., 1991. - Süsswasserflora von Mitteleuropa. Bacillariophyceae. 2/3: Centrales, Fragilariaceae, Eunotiaceae. G. Fischer Verlag, Stuttgart, 576 p.
KRAMMER K. & LANGE-BERTALOT H., 1991. - Süsswasserflora von Mitteleuropa. Bacillariophyceae. 2/4: Achnanthaceae. G. Fischer Verlag, Stuttgart, 437 p.
KRAMMER K. & LANGE-BERTALOT H., 2000. - Süsswasserflora von Mitteleuropa. Bacillariophyceae. 2/5: English and French translation of the keys. G. Fischer Verlag, Stuttgart, 311 p. Ce volume est la traduction française des clés de détermination.
| retour
en haut de page |
F. LA METHODE DES SAPROBIES (Sladecek, 1987, modifié)
Les indices qui donnent le plus de satisfaction dérivent tous de la méthode des saprobies de SLADECEK (1973, revu en 1987 pour les diatomées) basée sur la description des exigences écologiques vis-à-vis de la pollution. Elle consiste à tracer des spectres écologiques pour chaque espèce et à les décrire par deux critères :
- une "valence saprobique" quantifiant la sensibilité de l'espèce à la pollution organique : cette valence varie en continu de 5 pour les espèces très sensibles à 1 pour les espèces très résistantes (ou l'inverse dans Sladecek);
- une "valeur indicatrice" qui pondère l'indice et varie par unité de 5 pour une très bonne indicatrice à 1 pour une très mauvaise indicatrice.
Un exemple théorique de spectre écologique est donné à la figure 6. On place en ordonnée le pourcentage d'abondance d'une espèce dans les différentes classes de pollution définies au chapitre IPO (2.1.4.A.) et en abscisse les limites de ces classes. Dans l'exemple choisi, les exigences des l'espèces 1, 2 et 3 peuvent être décrites par une valence saprobique de 3 (préférence pour les milieux modérément pollués : 76 à 250 µg-P/l) mais l’espèce 1 reçoit une valeur indicatrice de 5 (très bonne indicatrice puisque son développement est pratiquement limité à une seule classe de qualité), l'espèce 2, une valeur indicatrice de 3 et l’espèce 3, une valeur indicatrice de 1 indiquant qu’elle est mauvaise indicatrice puisqu’elle est plutôt indifférente au phosphates (spectre plat). Enfin, l’espèce 4 reçoit une valence saprobique de 5 (préférence pour les milieux non pollués avec moins de 15 µg-P /l) et une valeur indicatrice de 5 (très bonne indicatrice).

Figure 6.- Exemple théorique de spectre écologique vis-à-vis des phosphates.
Il est à noter que de pareils spectres peuvent être tracés pour tous les paramètres chimiques. Voyons maintenant en pratique comment on détermine la valence saprobique par calcul du barycentre (figure 7).
On note tout d’abord qu’en abscisse sont placées les 5 classes de qualité : xénosaprobe, oligosaprobe, béta-mésosaprobe, alpha-mésosaprobe, polysabrobe. En ordonnée, les pourcentages d’abondance relative. Le tracé de ce type de spectre nécessite un grand nombre d’analyses chimiques et de comptages d’organismes en parallèle.
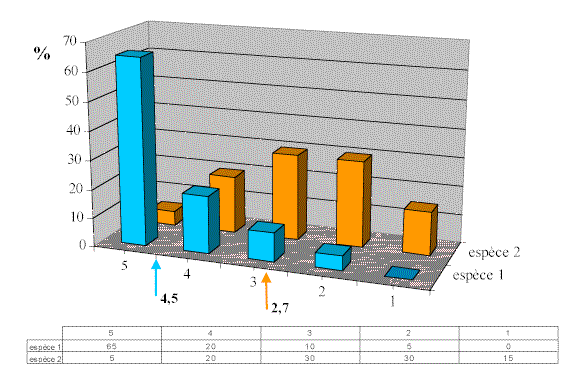
Figure 7.- Spectre écologique théorique.
L’espèce 1 présente une préférence pour la classe de qualité 5 (pollution nulle) avec un développement aussi dans la classe 4.
Sa valence saprobique = ((5x65) + (4x20) + (3x10) + (2x5) + (1x0)) /100 = 4,45
L’espèce 2 a un optimum dans la classe 3 mais est aussi bien présente dans la classe 2.
Sa valence saprobique = ((5x5) + (4x20) + (3x30) + (2x30) + (1x15))/100 = 2,70
Conventionnellement d’après Sladecek, la séquence distributive de l’espèce 1 (7 :2 :1 :0 :0 pour 65 :20 :10 :5 :0 %) correspond à une valeur indicatrice de 4 (bonne indicatrice, spectre étroit). La séquence de 0 :2 :3 :3 :2 (pour 5 :20 :30 :30 :15 %) de l’espèce 2 correspond à une valeur indicatrice de 2 (mauvaise indicatrice, spectre large).
Les espèces peuvent ainsi être groupées en 5 catégories écologiques suivant leur valence saprobique :

Figure 8. Groupes écologiques de diatomées.
| retour
en haut de page |
G. CALCUL DE L’INDICE DIATOMIQUE
Le tableau suivant donne les résultats d’un comptage. Il s’agit évidemment d’un exemple très simplifié, le nombre d’espèces étant limité à 5 alors que, généralement, il y en a plusieurs dizaines.
|
numéro de champ (voir figure 5) |
|||||||
|
1 |
5 |
9 |
13 |
etc |
total |
% |
|
|
espèce 1 |
30 |
20 |
15 |
30 |
… |
328 |
62,5 |
|
espèce 2 |
2 |
5 |
2 |
7 |
… |
64 |
12,2 |
|
espèce 3 |
0 |
1 |
1 |
0 |
… |
8 |
1,5 |
|
espèce 4 |
0 |
0 |
1 |
0 |
… |
4 |
0,8 |
|
espèce 5 |
13 |
5 |
12 |
7 |
… |
120 |
23,0 |
|
TOTAL |
524 |
100 |
|||||
Le calcul de l’indice diatomique pondéré de qualité d’eau est donné par la formule suivante :
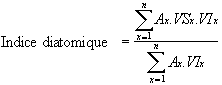
où n est le nombre d’espèces, A l’abondance relative, vs et vi, la valence saprobique et la valeur indicatrice.
La tableau donne les vs et vi pour notre exemple.
|
Espèce |
Abondance en % |
vs |
vi |
|
1 2 3 4 5 |
62,5 12,2 1,5 0,8 23,0 |
4,0 2,1 5,0 1,0 2,9 |
5 2 5 2 1 |
Indice diatomique d’après le calcul suivant (moyenne pondérée) :
![]()
Différents auteurs ont publié des listes d’espèces assorties de leurs valences et valeurs indicatrices (SLADECEK, 1973 ; MOUTHON & COSTE, 1984 ; SLADECEK, 1986 ; LECLERCQ & MAQUET, 1987 ; LECLERCQ, non publié).
Sur base d’une comparaison de différentes méthodes chimiques et biologiques (LECLERCQ & MAQUET, 1987), nous avons montré que les indices actuellement les plus précis avaient été publiés, avec des listes d’espèces, dans :
SLADECEK V., 1986. – Diatoms as indicators of organic pollution. Acta Hydrochimica et Hydrobiologica, Dresden 14(5) : 555-566.
LECLERCQ L. & MAQUET B., 1987. – Deux nouveaux indices chimique et diatomique de qualité d’eau courante. Application au Samson et à ses affluents (Bassin de la Meuse belge). Comparaison avec d’autres indices chimiques, biocénotiques et diatomiques. Inst. Roy. Sc. Nat. Belg., Document de travail 38 : 113 p.
LECLERCQ L., 2000 (non publié, 450 espèces).
Ajoutons la méthode de l’IBD (indice biologique diatomées) qui vient d’être normalisé en France. Dans le guide technique de cette norme, publié par les Agences de l’Eau, on trouve, outre des clés d’identification des espèces les plus importantes, toutes illustrées, un CD-Rom permettant le calcul de plusieurs indices.
| retour
en haut de page |
H. INTERPRETATION GLOBALE DES INDICES DIATOMIQUES
Les valeurs indicielles sont généralement réparties en 5 classes, d'étendue différente suivant chaque méthode. Ces classes correspondent aux niveaux de pollution décrits dans SLADECEK (1973) par des termes que l'on trouve couramment dans la littérature et donnés dans la deuxième colonne du tableau ci-dessous. Les classes de valeurs indicielles données ici ont été établies par LECLERCQ & MAQUET (1987) :
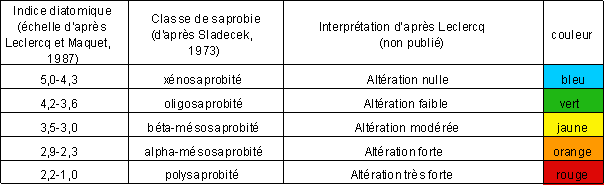
Dans l'exemple donné ci-dessus, l'indice pondéré de 3,8 correspond à une altération faible.
| retour
en haut de page |
I. INTERPRETATION APPROFONDIE DES INDICES DIATOMIQUES
Nous avons vu dans le chapitre " Méthodes chimiques " qu’à partir du point de rejet de l’égout, on assistait à une transformation progressive des matières organiques en matières minérales (nitrates et phosphates). Il est donc important de bien distinguer ces deux états.
Des indices inférieurs à 2,3 (altération très forte) sont obtenus pour des peuplements dominés par les espèces très résistantes (groupe 1). Par contre, des indices entre 2,5 et 3,5 sont obtenus pour des situations très variées, constituées d’un mélange d’espèces hypereutrophes (groupe 3) et (groupe 2).
Les diatomées permettent donc de faire la différence entre ces deux états de la pollution. Pour ce faire, on totalise les abondances des espèces de même écologie (voir les 5 groupes de la figure 10).
Pour l’eutrophisation, nous proposons la table d’interprétation suivante, la couleur verte de plus en plus intense indiquant une augmentation progressive de la biomasse végétale en raison des concentrations croissantes en nutriments.

Voici un exemple de fiche d’interprétation approfondie
|
Groupe 5+4 |
44,6 % |
DBO5 |
- |
mg-O2/l |
|
|
Groupe 3 |
33,3 % |
NH4+ |
0,0 |
mg-N/l |
|
|
Groupe 2 |
20,5 % |
NO2- |
11 |
m g-N/l |
|
|
Groupe 1 |
1,6 % |
NO3- |
5,6 |
mg-N/l |
|
|
Groupe 0: écologie inconnue |
0,0 % |
PO4--- |
3 |
m g-P/l |
|
|
3,6 |
4,3 |
|||
|
faible |
faible |
|||
|
Groupe 3 |
33,3 % |
|
modérée |
|
|
Groupes 2 + 1 |
22,1 % |
|
faible |
|
Niveau typologique
Les espèces sensibles, bien représentées dans cette station, sont principalement Achnanthes minutissima, Cocconeis placentula var. euglypta et Cymbella sinuata, espèces présentes dans les eaux de type oligo-mésotrophes typiques du Dévonien inférieur.
Pollution organique
Les 22,1 % d'espèces résistantes indiquent une pollution organique est faible.
Eutrophisation
33,3 % d’espèces du groupe 3 indiquent une eutrophisation modérée. Ce sont principalement Achnanthes lanceolata, Navicula minima et Navicula lanceolata. Cette eutrophisation provient des prairies amendées que traverse le cours d’eau.
Bilan
La station est modérément hypertrophisée par l'environnement agricole. Une faible pollution organique s’y ajoute.
Pour la pollution organique, nous proposons la table d’interprétation suivante : il n’y a pas de couleur associée ici car on peut avoir, par exemple, une altération modérée (en jaune) qui correspond à la juxtaposition d’une pollution organique faible et d’une eutrophisation modérée.

| retour
en haut de page |
J.1. Distinguer pollution organique et eutrophisation, essentiel pour la gestion des eaux…
Voici, comme exemple, la composition moyenne annuelle (1987) des peuplements de diatomées dans 5 stations de la Joncquière et la comparaison avec la chimie des eaux de cette rivière qui a déjà été présentée au chapitre 2.1.4.D.
Un très bon parallèle apparaît entre les groupes dominants de diatomées (mis en couleur en fonction de leur écologie) et l’état chimique parce qu’on dispose de moyennes annuelles soit une analyse chimique par moi.
A la station 1, en amont du village, on est en zone agricole intensive : il en résulte la disparition des espèces très sensibles au profit des espèces d’eau faiblement polluée indiquant une contamination faible mais rémanente par lessivage des prés amendés ainsi que le montrent les phosphates (35 µg-P/l au lieu de moins de 15 en situation naturelle). Par ailleurs, après le rejet, la succession des espèces " rouges, oranges, jaunes puis vertes " indique bien l’autoépuration.
L’évolution chimique suit le schéma classique : diminution progressive du phosphore, maximum de l’ammonium à la station 3 (1,5 km après le rejet), puis maximum des nitrites en station 4 et des nitrates en 6, au fur et à mesure de l’oxydation.
Ainsi, les diatomées sont les seuls organismes capables de faire précisément et de façon intégrée, la distinction entre les différentes formes de pollution organique et l’eutrophisation, les peuplements étant très différents dans ces deux cas. Essentiel donc pour la gestion de l’eau !

| retour
en haut de page |
J.2. La preuve que les diatomées intègrent…
Une rivière a été suivie, chaque mois, par des analyses chimiques et diatomiques. On a donc calculé les IPO (indice de pollution organique) et les indices diatomiques. Comme généralement, les prélèvements chimiques étaient momentanés. La figure ci-dessous montre les variations de ces deux indices.
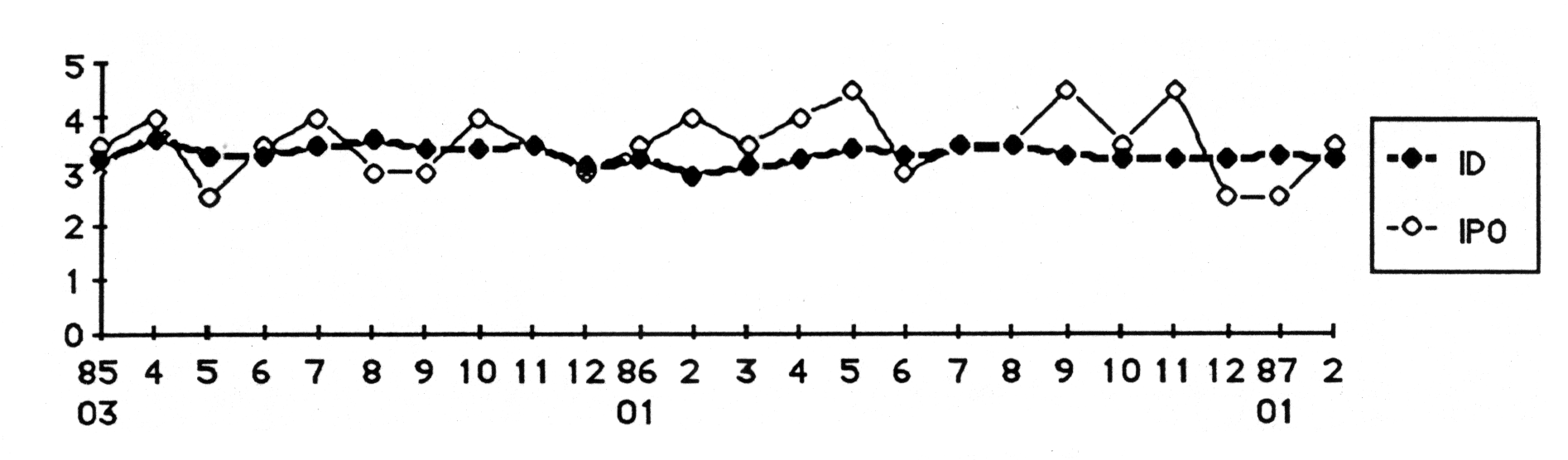 Figure
9. - Variations mensuelles des indices diatomiques et de pollution organique
dans une station eutrophiquée de la Wimbe (prov. Namur, Belgique).
Figure
9. - Variations mensuelles des indices diatomiques et de pollution organique
dans une station eutrophiquée de la Wimbe (prov. Namur, Belgique).
L'indice de pollution organique (IPO) fluctue constamment entre les niveaux de pollution faible à forte. Par contre, 85% des indices diatomiques correspondent à une pollution modérée.
D’autre part, si on calcule l’IPO moyen annuel, sa valeur de 3,0 se classe exactement dans le même niveau de pollution modérée que chacun des indices diatomiques mensuels.
La capacité intégratrice des diatomées est ainsi démontrée et permet donc d'obtenir une bonne estimation à partir d'un seul prélèvement par an alors que le prélèvement chimique doit être répété. Le graphique peut permettre d’évaluer statistiquement le nombre de prélèvements d’eau nécessaires pour obtenir la bonne estimation de qualité.
Evidemment, ce raisonnement ne peut être appliqué que pour des agglomérations dont la charge polluante est globalement identique tout le long de l’année. La présence d’activités touristiques importantes (campings, grands complexes hôteliers,…) est la cause de fortes variations des charges polluantes : il est alors nécessaire de répéter aussi quelques fois les prélèvements de diatomées, au moins avant, au milieu et un mois après la saison touristique.
De même, quand on se trouve très proche d’un point de rejet dont le débit peut être aussi important que celui du cours d’eau en étiage, il faut s'attendre à des variations plus importantes de l'indice diatomique, dues aux variations saisonnières (impact de la température sur l'autoépuration, dilution ou concentration des polluants en fonction des débits). Dans ces conditions, il est nécessaire de prélever au moins trois fois par an (soit dans des conditions de débit normal, d'étiage estival et de crues hivernales de longue durée).
Dans tous les cas , il faudra procéder à un nombre supérieur de prélèvements d’eau.
| retour
en haut de page |
J.3. Les diatomées sont hypersensibles…
Les indices diatomiques et de pollution organique sont assez stables dans des conditions naturelles ou proches de l'état naturel. Cependant, dans un environnement agricole, l'IPO est généralement plus élevé (pollution nulle à faible) que l'Indice diatomique (pollution faible à modérée).
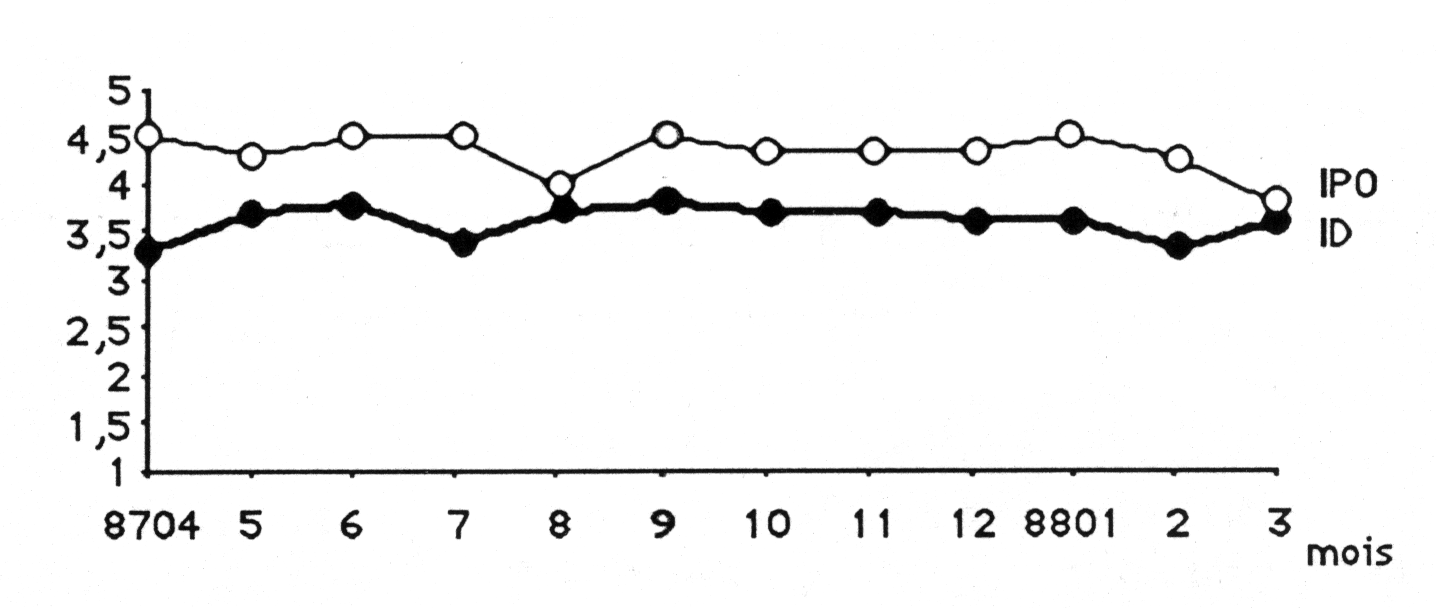
Figure 10. - Comparaison des indices diatomiques (en noir) et de pollution organique (en blanc) dans une station en zone agricole (Joncquière, station 413).
Ainsi, la contamination faible mais permanente par lessivage des amendements agricoles est difficilement révélée par l’analyse chimique mais ce faible apport en phosphore et azote est directement assimilé par la biomasse qui augmente. Par contre, au niveau des peuplements de diatomées, cet apport suffit à faire régresser les espèces très sensibles et à provoquer une diminution de l’indice.
Ce type d'altération est de plus en plus répandu, marquant une tendance généralisée à l'eutrophisation des eaux de surface et souterraines. On commence à prendre des mesures de réduction des amendements en aidant les agriculteurs, dans les Parcs Naturels notamment, à mieux estimer les doses à appliquer et les époques d’épandages. Trop souvent en effet, les épandages se font en hiver quand la végétation n’est pas active et même parfois sur sol gelé : le ruissellement de l’eau de pluie emmène alors une grande partie vers les cours d’eau.
| retour
en haut de page |
K. LES DIATOMEES, DIFFICILE ???
Comme ces organismes sont microscopiques, il est certes nécessaire de disposer d’un bon microscope (exemple : Zeiss, un objectif à immersion, environ 1500 Euros). L’identification des espèces nécessite par ailleurs des ouvrages spécialisés.
MAIS…
Il existe une méthode simplifiée.
Ses avantages :
- on identifie seulement les genres, soit une trentaine pour les eaux douces courantes, avec une clé simplifiée bine illustrée ;
- on suit la méthode des saprobies décrite ci-dessus et qui, nous l’avons vu, donne les meilleurs résultats pour l’évaluation des pollutions organiques et de l’eutrophisation.
Référence de cette méthode :
RUMEAU A. & COSTE M., 1988. - Initiation à la systématique des diatomées d'eau douce. Bull. Fr. Pêche Piscic., 309 : 1-69.
Nom de l’indice : indice diatomique générique (IDG).
Certes, ce n’est pas parfait car on sait qu’attribuer une signification écologique à un genre constitue une perte d’information parfois importante puisque dans chaque genre, on trouve des espèces d’écologie parfois très variée.
Toutefois, l’approche est intéressante et conduit souvent à une évaluation acceptable.
Cette publication comprend une partie systématique présentée avec originalité : lexique illustré, clés non dichotomiques mais bien illustrées suivies de clés plus détaillées par sous-classes et ordres donnant en plus un aperçu de la variabilité des formes au sein de chaque genre : il est ainsi possible d'identifier la plupart des genres d'eau douce.
Ensuite, pour les genres, éventuellement scindés en sections, les auteurs donnent des valences saprobiques et des valeurs indicatrices, l'indice diatomique générique étant alors calculé à partir de la même formule mathématique que celle citée ci-dessus (chapitre 2.3.2.1.G.).
| retour
en haut de page |
Nous l'avons dit plus haut, les peuplements de diatomées se modifient dès que le niveau des sels dissous (calcium, magnésium, chlorures, sodium, potassium,…) augmente naturellement : on connaît d'ailleurs assez bien les affinités écologiques des espèces d'eau douce vis à vis du calcium.
Mais en outre, il existe, dans la littérature, assez bien d'indications concernant le comportement de ces espèces vis à vis des chlorures (VAN HEURCK, 1880-1885; HUSTEDT, 1957; VAN DER WERFF & HULS, 1957-1974; PIERRE, 1965-1968-1969; GERMAIN, 1981).
L'idée nous est donc venue d'utiliser les diatomées comme indicateurs de salinité pour étudier l'impact de rejets salins divers dont notamment les sels de déneigement. A ce propos, les récents hivers peu enneigés font que les études ne sont pas encore assez avancées pour signaler ici des exemples probants. Par contre, l'impact d'un rejet salin bien défini a été étudié avec succès par cette méthode : nous le citerons comme exemple.
Par analogie au système des saprobies, on utilise le terme d'halobie pour caractériser l'écologie des diatomées vis à vis des chlorures. Nous avons retenu la classification de VAN DER WERFF & HULS (1957 - 1974) qui définit des espèces d'eau douce (Z = zoet), d'eau saumâtre (B = brak) et d'eau salée (M = marien). Ces classes correspondent plus ou moins à des zones de développement optimal ce qui n'exclut évidemment pas qu'une espèce de type Z puisse être observée et même atteindre un développement limite dans les classes ZB ou BZ : la notion d'amplitude écologique est ici aussi d'application !
Voici les limites de classes que nous adoptons :
|
Classe |
Type d'eau |
Teneurs en Cl- mg/l |
Salinité totale mg/l |
|
Z ZB B BM MB M |
Eau douce Eau douce Eau légèrement saumâtre Eau saumâtre Eau fortement saumâtre Eau salée Eau de mer |
<100 100-500 500-1000 1000-5000 5000-10000 10000-17000 >17000 |
<180 180-900 900-1800 1800-9000 9000-18000 18000-30000 >30000 |
Les sommes des abondances relatives des espèces d'eau douce (Z + ZB), d'eau saumâtre (BZ + B + BM) et d'eau salée (MB + M) seront utilisées pour caractériser chaque station.
Il reste alors à déterminer, à partir de ces 3 pools d'espèces, dans quelle mesure le peuplement peut s'adapter à une éventuelle augmentation de la salinité et à en fixer le niveau maximum.
Exemples : impact de rejets salins
Il s'agit d'un établissement thermal rejetant des eaux salées pompées en profondeur. L'eau du pompage a une salinité de 8000 mg/l de chlorures (notre zone BM : eau fortement saumâtre). Nous avons prélevé dans la rivière avant et après le rejet (stations 1 et 3) et dans un canal ou une partie du rejet transite (station 2). Voici le tableau de synthèse des comptages de diatomées (en % d'abondance relative) :
|
N° station |
classes de salinité |
Z + ZB eau douce |
BZ + B + BM |
Cl- mg/l |
||||
|
Z |
ZB |
BZ |
B+BM |
MB+M |
eau saumâtre |
|||
|
1 |
29 |
67 |
1 |
3 |
0 |
96 |
4 |
26 |
|
2 |
10 |
46 |
38 |
6 |
0 |
56 |
44 |
8000 |
|
3 |
22 |
61 |
1 |
16 |
0 |
83 |
17 |
39 |
On voit donc clairement se développer des espèces adaptées à des salinités plus élevées alors qu'apparemment, l'augmentation des chlorures est faible (de 26
à 39 mg/l). Il faut voir là l'effet intégrateur des diatomées car, au moment du prélèvement, le débit du rejet salin dans le canal était manifestement très réduit. La flore diatomique dans ce canal indique par ailleurs la réalité du rejet.
Dans le même ordre d'idée, voici les peuplements de diatomées d'une rivière qui reçoit les eaux de percolation d'un terril : ces eaux sont très chargées en sels dissous ainsi qu'en témoignent les précipités de carbonates et de sels de fer. La station 1 se situe en amont du rejet, la station 3, 4 km en aval et la station 2 dans le rejet lui-même.
|
n° station |
classes de salamité |
Z+ZB eau douce |
BZ + B + BM eau saumâtre |
||||
|
Z |
ZB |
BZ |
B+BM |
MB+M |
|||
|
1 2 3 |
11 0 2 |
82 2 5 |
3 34 32 |
4 64 61 |
0 0 0 |
93 2 7 |
7 98 93 |
Dans ce cas, l'impact est beaucoup plus marqué, le débit du rejet étant au moins égal à celui du ruisseau.
| retour
en haut de page |
M. AVANTAGES DES INDICES DIATOMIQUES
L'expérience nous a montré que le principal avantage était la fiabilité et la précision des résultats obtenus, face à la variabilité des autres indices. Cet avantage découle de la sensibilité de ces algues aux polluants eux-mêmes, notamment les formes de l'azote et du phosphore et les chlorures, de la faible influence de facteurs étrangers à la pollution tels que le type de substrat et de leur capacité d'intégration à moyen terme.
Plus particulièrement, il existe des groupes d'espèces permettant de déterminer le niveau trophique naturel d'une station, les différentes étapes suivant une pollution organique (successivement, la contamination par l'ammonium et les phosphates, par les nitrites et les phosphates, et par les nitrates et les phosphates) et enfin les niveaux de salinité. La contamination par le lessivage d'engrais en zone agricole est aussi repérable.
Ces résultats indiquent les domaines d'application des indices diatomiques : inventaire des eaux naturelles et polluées, surveillance des réseaux hydrographiques, surveillance de la qualité des rejets des stations d'épuration.
Le deuxième avantage est évidemment la capacité intégratrice de ces organismes : nous l'estimons à environ 3 semaines précédant le jour de prélèvement. Un indice diatomique fournit donc une estimation qui correspond à la moyenne d'analyses chimiques qui seraient réalisées pendant une vingtaine de jours consécutifs.
De ce deuxième avantage en découlent deux autres : le prix avantageux d'un indice diatomique par rapport à 20 prélèvements pour analyse chimique et la possibilité d'établir un réseau de surveillance plus vaste et (ou) une densification des stations de prélèvement, tout en garantissant des résultats aussi fiables.
Soulignons encore la simplicité et la rapidité du prélèvement, la possibilité de récolter ces organismes pratiquement partout, l'espace de stockage réduit (par exemple, sous forme d'une collection de préparations microscopiques définitives), la possibilité de constitution d'une banque de données rassemblant les résultats des comptages et le calcul des indices.
| retour
en haut de page |
Le principal inconvénient est la nécessité d'identifier les organismes jusqu'à l'espèce ce qui demande un traitement spécial de l'échantillon, son observation avec un microscope de qualité, l'achat de quelques ouvrages de base (dont nous avons donné la référence) et enfin, une période de formation de quelques mois.
Certains auteurs ont mis au point des méthodes simplifiées mais, quelque soit le soin apporté à leur élaboration, la perte d'information reste élevée. L'identification au genre permet surtout de réduire l'acquisition d'ouvrages spécialisés et coûteux et l'équipement microscopique (pas de dispositif de mesure de taille, de nombre de stries,…).
Enfin, dans l'état actuel des connaissances, les pollutions minérales, mis à part les rejets salins (surtout les chlorures) ne peuvent pas être valablement estimées par les diatomées.
| retour
en haut de page |
![]()