![]()
B.1.1. Les hydrogénocarbonates HCO3- et les carbonates CO32-
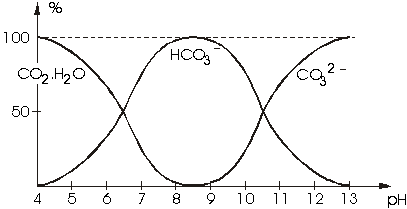
La présence de CO2 et des ions carbonatés dépend fortement du pH de l'eau. Le graphique suivant illustre les courbes théoriques de pourcentage de chaque espèce en fonction du pH.
![]() Dosage des ions CO32-
Dosage des ions CO32-
Ces ions ne sont présents en concentration mesurable que dans les eaux dont le pH est supérieur à 8.
Le titre alcalimétrique (T.A.) est le volume d'acide à 0,02 mol/l d'ions H3O+ nécessaire pour doser 100 ml d'eau en présence de phénolphtaléine.
Méthode de dosage.
On introduit dans 100 ml de solution quelques gouttes de phénolphtaléine (zone de virage de 8,2 à 10 unités de pH). Celle-ci vire au rouge. On titre par H2SO4 0,01 M jusqu'à décoloration de l'indicateur, selon la réaction :
CO32- + H3O+HCO3- + H2O.
On calcule ensuite la concentration en carbonate.
![]() Dosage des ions HCO3-
Dosage des ions HCO3-
Ces ions constituent la forme la plus abondante sous laquelle on trouve le carbone minéral dans les eaux naturelles.
Le titre alcalimétrique complet (T.A.C.) est le volume d'acide à 0,02 mol/l d'ions H3O+ nécessaire pour doser 100 ml d'eau en présence de vert de bromocrésol.Méthode de dosage.
Il s'agit d'un titrage acide-base suivant l'équation :
HCO3-+ H3O+H2CO3 + H2O
2 H2O + CO2
On ajoute à 100 ml d'eau quelques gouttes de l'indicateur vert de bromocrésol (zone de virage de 3,8 à 5,4 unités de pH) et on titre par une solution de H2SO4 0,01 M jusqu'au changement de couleur du bleu au jaune. Le titrage doit être réalisé avec une forte agitation pour éliminer le gaz CO2. Un chauffage à 50°C favorise également cette élimination.La concentration en ions HCO3- peut alors être calculée.
B.1.2. La dureté totale en Ca2+ et Mg2+
La dureté d'une eau représente la concentration en ions calcium et magnésium. La dureté d'une eau de rivière dépend essentiellement des sols qu'elle rencontre. Si une eau a une dureté élevée, on retrouvera rapidement des dépôts de calcaire en la chauffant pour les usages domestiques (bouilloires, chauffe-eau ...). Les produits adoucissants que l'on trouve dans les poudres à lessiver (et qui aboutissent dans les rivières) complexent ces ions pour les maintenir en phase aqueuse.
![]() Dosage des ions Ca2+ et Mg2+ par le coffret
Merck
Dosage des ions Ca2+ et Mg2+ par le coffret
Merck
La méthode Merck de mesure de la dureté totale de l'eau est un titrage utilisant une réaction de complexation.
Les équations de la réaction sont celles qui sont présentées ci-après dans le mode opératoire proposé pour un dosage avec le matériel de laboratoire.Mode d'emploi
1. Rincer le tube à essais avec l'eau à analyser et le remplir jusqu'au repère de 5 ml.
2. Ajouter 3 gouttes de solution indicatrice et agiter. En présence de générateurs de
dureté, l'échantillon se colore en rouge.
3. Poser simplement la pipette de titrage et en tirant lentement, remplir la seringue
avec la solution de titrage jusqu'à ce que le bord inférieur du joint noir du piston
corresponde à la division 0° dH de l'échelle.
4. Enlever la pipette de titrage, frotter brièvement l'extrémité du tube compte-gouttes.
A l'échantillon d'eau préparé, ajouter alors la solution de titrage jusqu'à ce que la
couleur de l'échantillon d'eau vire du rouge au vert en passant par le gris-violet
(peu de temps avant le virage). Ce faisant, agiter le tube à essai.
5. Lire la dureté totale de l'eau en mmol/l ou en °d sur l'échelle correspondance de
la pipette de titrage.
6. Lorsque l'analyse est terminée, repousser le piston de la pipette de titrage vers
le bas et bien revisser celle-ci sur le flacon de réactifs.
![]() Dosage au laboratoire des ions Ca2+ et Mg2+
dans l'eau par complexométrie
Dosage au laboratoire des ions Ca2+ et Mg2+
dans l'eau par complexométrie
a) Description de la réaction
Le complexant utilisé est un sel de l'acide éthylènediaminetétraAcétique (EDTA), que l'on peut représenter par Na2H2Y.La réaction de complexation s'écrit :
Ca2+ + H2Y2-CaY2- + 2H+
Mg2+ + H2Y2-MgY2- + 2H+
Avant l'addition d'EDTA, un autre complexant de Ca2+ et Mg2+, le noir d'ériochrome T (NET) est ajouté en très faible quantité à la solution, pour jouer le rôle d'indicateur. II forme avec les ions Ca2+ et Mg2+, des complexes de couleur rouge CaNET- et MgNET-.
Pendant le titrage, l'EDTA ajouté complexe progressivement les ions Ca2+ et Mg2+ de la solution.
Au terme du titrage, les complexes CaNET- et MgNET- disparaissent et le noir d'ériochrome libre apparaît dans la solution avec sa couleur bleue.
II est nécessaire de travailler en milieu tampon basique (pH = 9,5) pour observer correctement les changements de couleur.Mode opératoire
- Introduire dans un erlenmeyer de 25O ml, 50 ml de la solution à analyser.
- Chauffer jusqu'à environ 60°C.
- Ajouter 10 ml de la solution tampon destinée à fixer le pH.
- Ajouter une faible quantité de NET.
- Titrer par la solution d'EDTA 0,002 M jusqu'au virage du rouge au bleu.b) Dosage des ions Ca2+ seuls
Lorsque le pH est au moins égal à 12, l'EDTA ne réagit qu'avec les ions Ca2+. Les ions Mg2+ précipités sous forme de Mg(OH)2 ne sont pas dosés.
II faut alors utiliser le murexide comme indicateur.Mode opératoire
- Prélever 50 ml de solution à analyser.
- Ajouter 5 ml d'une solution de NAOH 0,1 M pour obtenir un pH =12
- Ajouter une faible quantité de murexide.
- Titrer rapidement par la solution d'EDTA jusqu'au virage du rose au bleu.c) Calcul de la concentration en ions Mg2+
La concentration en ions Mg2+ s'obtient par différence à partir des résultats des titrages précédents, en exprimant toutes les concentrations en moles/litre.
d) Application aux eaux de rivière
Les concentrations usuelles sont exprimées en mg/litre.
La concentration en ions d'une rivière de type ardennais comme l'Ourthe varie entre 20 et 60 mg/l pour Ca2+ et entre 2 et 10 mg/l pour Mg2+.
B.1.3. Les ions chlorures
Des ions chlorures d'origine géologique sont présents dans toutes les eaux naturelles: les eaux souterraines normales contiennent entre 5 et 30 mg/l de Cl-.
Les chlorures comme le chlorure de calcium, de sodium assurent avec les carbonates l'équilibre minéralogique des rivières. Une perturbation grave de cet équilibre entraîne des problèmes de croissance et de développement des végétaux aquatiques.
Les chlorures peuvent exister en concentrations élevées d'origine humaine (urine) ou industrielle (industries extractives, industries métallurgiques,...).
Une eau est considérée comme polluée au-dessus de 200 mg/l.
La présence excessive de Cl- dans l'eau favorise la corrosion des métaux, la rend impropre à l'irrigation, à la vie végétale et animale.
![]() Dosage des chlorures par le coffret Merck
Dosage des chlorures par le coffret Merck
Le coffret Merck propose un titrage par réaction avec une solution de nitrate de mercure :
2 Cl- + Hg2+HgCl2
Le chlorure de mercure HgCl2 n'est pratiquement pas dissocié dans l'eau. En solution nitrique, les ions Hg2+ en excès forment avec la diphénylcarbazone, servant d'indicateur, un complexe bleu-violet.Mode d'emploi
1. Rincer le récipient à essais avec l'eau à analyser et le remplir jusqu'au repère (correspondant à 5 ml).
2. Ajouter 2 gouttes du Réactif 1 (solution indicatrice) et agiter soigneusement. En général, la solution prend une coloration bleue.
3. Continuer à agiter en ajoutant goutte à goutte le Réactif 2 (acide nitrique), jusqu'au virage au jaune.
4. Poser simplement la pipette de titrage et la remplir en tirant le piston de la seringue lentement vers le haut jusqu'à ce que le bord inférieur du joint noir du piston coïncide avec la graduation 0 mg/l de l'échelle.
5. Enlever la pipette de titrage. Frotter brièvement la pointe du compte-gouttes. Ajouter alors la solution de titrage (Réactif 3) goutte à goutte à l'échantillon d'eau préparé, en agitant le récipient à essais constamment jusqu'à ce que la couleur de l'échantillon d'eau vire du jaune au violet.
6. Lire la teneur en chlorures de l'eau en mg/l sur l'échelle de la pipette de titrage.
7. A la fin de l'analyse, pousser le piston de la pipette de titrage vers le bas et bien visser celle-ci sur le flacon à réactifs.Le dosage des chlorures peut aussi être effectué avec une solution de nitrate d'argent en repérant le point équivalent par potentiométrie.
![]() Dosage des ions CI- par potentiométrie
Dosage des ions CI- par potentiométrie
a) Description de la méthode
Les ions Cl- réagissent avec des ions Ag+ suivant la réaction de précipitation :
Ag+ + Cl-AgCl (solide)
Le produit de solubilité Kps relie la concentration de ces ions en solution :
Kps = [ Ag+ ] . [ Cl- ]
La relation entre la concentration des ions Ag+ et la concentration des ions Cl- est :
[ Ag+ ] = Kps / [ Cl- ]
Le potentiel d'une électrode d'argent plongée dans une solution dépend donc de sa concentration en ions Cl- :
EAg = E°Ag+/Ag + 0,059 log [ Ag+ ]
EAg = E°Ag+/Ag + 0,059 log Kps / [ Cl- ]Lorsqu'on ajoute progressivement une solution de AgNO3 à la solution contenant des ions Cl-, ceux-ci disparaissent par formation du précipité AgCl. Le potentiel de l'électrode d'argent augmente avec un saut brusque au moment où il y a égalité des concentrations des ions Ag+ et Cl-.
Le saut de potentiel permet de repérer le point équivalent dans un graphique reliant le potentiel de l'électrode et le volume de solution de AgNO3 ajouté.b) Mode opératoire
Placer dans un bécher 100 ou 200 ml d'eau à analyser.
Plonger dans l'eau une électrode d'argent et relier le bécher à une électrode de référence par un tube en U contenant KNO3 pour réaliser un pont électrolytique. Mesurer le potentiel de l'électrode d'argent avec un millivoltmètre électronique. Ajouter des volumes de 0,5 ml de solution de AgNO3 5.10-3 M et noter le potentiel. Tracer la courbe du potentiel en fonction du volume de AgNO3 ajouté et prendre le volume équivalent au milieu du saut de cette courbe.
Calculer la concentration des ions Cl- en moles/l et en g/l.
B.1.4. Les phosphates
La plus grande partie des phosphates présents dans l'eau de rivière provient du lessivage des sols agricoles enrichis en engrais, des rejets des eaux domestiques et des activités industrielles.
Les phosphates réagissent avec les ions calcium présents dans les rivières et modifient les équilibres naturels. De plus, ils permettent la prolifération d'algues qui consomment le dioxygène présent dans l'eau et provoquent le phénomène d'eutrophisation : la disparition de la vie dans la rivière par asphyxie.
Les phosphates sont utilisés pour complexer le calcium et permettre l'action des détergents dans les poudres à lessiver (adoucissants). L'introduction sur le marché de lessives écologiques, c'est-à-dire sans phosphate a eu aussi des effets pervers. En effet, on peut trouver dans ces lessives "vertes" du NTA (acide nitrilo-tri-acétique) qui complexe le calcium, même à 90 °C, et qui est soupçonné d'entraîner les métaux lourds des rivières vers les nappes souterraines. On y trouve également de l'EDTA, (acide éthylènediamine tetracétique) suspecté d'être très toxique dans les rivières. Enfin ces lessives contiennent des zéolithes (alumino-silicates, bref des argiles) non toxiques qui captent aussi le calcium; cependant, pour obtenir les mêmes propriétés que les polyphosphates, il faut ajouter des tensioactifs qui sont aussi polluants et dévoreurs d'oxygène...
![]() Dosage des phosphates avec le réflectomètre Merck
Dosage des phosphates avec le réflectomètre Merck
La détermination de la totalité du phosphore contenu dans l'eau nécessite des manipulations relativement longues : on se limitera au dosage des orthophosphates ( PO43-) par une méthode colorimétrique.
Mode opératoire
Suivre le manuel du réflectomètre RQflex plus.
Pour le Test Phosphates :
Procédure E (pour le dosage en cuves)
Temps de réaction mémorisé : 5 secondes.
Préparer l'échantillon à mesurer et l'échantillon à blanc :
|
..
|
Echantillon à mesurer
|
Echantillon à blanc
(1 seul par série) |
..
|
| Echantillon préparé (20 ( 30° C) |
5 ml
|
5 ml
|
Remplir le tube à essai jusqu'au repère de 5 ml |
| Réactif PO4-1 |
5 gouttes
|
---
|
Ajouter prudemment et mélanger |
| Réactif PO4-2 | 1 microcuiller bleue arasée (fixée dans le bouchon du flacon PO4-2) |
---
|
Ajouter et dissoudre en agitant |
| Pipetter l'échantillon à mesurer et l'échantillon à blanc à l'aide d'une pipette à usage unique différente dans deux cuves différentes et remplir les deux compartiments de chaque cuve jusqu'à la limite supérieure de la partie transparente. | |||
Mesure :
· Placer la cuve contenant l'échantillon à blanc dans le compartiment de mesure, refermer le capot et presser la touche START.
· Lorsque l'ordre s'en inscrit sur l'affichage, placer la cuve contenant l'échantillon à mesurer dans le compartiment de mesure, refermer le capot et presser de nouveau la touche START.
· Lire sur l'affichage le résultat d'analyse en mg/l de PO43-
· Le résultat est mémorisé automatiquement.
· Immédiatement après la mesure, retirer la cuve du compartiment de mesure.
B.1.5. Les sulfates
Les sulfates naturels de l'eau proviennent de la dissolution du gypse (CaSO4.2H2O) ou du lessivage des terrains contenant des pyrites dont les sulfures entraînés s'oxydent en sulfates à l'air.
Les concentrations inférieures à 200 mg/l ne posent pas de problèmes. Des concentrations supérieures provoquent la précipitation du sulfate de calcium dans les eaux calcaires. Des concentrations supérieures à 100 mg/l favorisent la corrosion des métaux.
La concentration admissible en sulfates pour l'homme est de 250 mg/l. Au delà de celle-ci, ils ont un effet laxatif excessif.
![]() Dosage des sulfates
Dosage des sulfates
La méthode traditionnelle de dosage des sulfates est la précipitation du sulfate de baryum et la détermination de la quantité de précipité par turbidimétrie:
Ba2+ (aqueux)
+ SO42-(aqueux) ![]() BaSO4 (solide)
BaSO4 (solide)
B.1.6. Les ions sodium et potassium
Ces ions positifs se trouvent en concentrations très variables dans les eaux naturelles. Le sodium peut être apporté en quantités importantes dans les rejets industriels ou domestiques (sel de cuisine ...).
![]() Dosage des ions K+ avec le réflectomètre Merck
Dosage des ions K+ avec le réflectomètre Merck
Mode opératoire
Suivre le manuel du réflectomètre RQflex plus.
Pour le Test Kalium :
Procédure E (pour le dosage en cuves)
Temps d'attente mémorisé : 300 secondes
Temps de réaction mémorisé : 5 secondes
Préparer l'échantillon à mesurer et l'échantillon à blanc :
|
..
|
Echantillon à mesurer
|
Echantillon à blanc
(1 seul par série) |
..
|
| Echantillon préparé (20 - 40 °C) |
5 ml
|
5 ml
|
Remplir le tube à essai jusqu'au repère de 5 ml |
| Réactif K-1 |
10 gouttes
|
---
|
Ajouter et mélanger |
| Réactif K-2 |
6 gouttes
|
---
|
Ajouter et mélanger |
| Réactif K-3 | 1 microcuiller bleue arasée (fixée dans le bouchon du flacon K-3) | .. | Ajouter et dissoudre en agitant, puis presser la touche START du réflectomètre |
| A la fin du temps d'attente (le temps de réaction apparaît sur l'affichage), agiter l'échantillon à mesurer, puis pipetter l'échantillon à mesurer et l'échantillon à blanc à l'aide d'une pipette à usage unique différente dans deux cuves différentes et remplir les deux compartiments de chaque cuve jusqu'à la limite supérieure de la partie transparente. | |||
Mesure :
· Placer la cuve contenant l'échantillon à blanc dans le compartiment de mesure, refermer le capot et presser la touche START.
· Lorsque l'ordre s'en inscrit sur l'affichage, placer la cuve contenant l'échantillon à mesurer dans le compartiment de mesure, refermer le capot et presser de nouveau la touche START.
· Lire sur l'affichage le résultat d'analyse en mg/l de K. Le résultat est mémorisé automatiquement.
· Immédiatement après la mesure, retirer la cuve du compartiment de mesure.
![]() Estimation de la concentration des ions Na+
Estimation de la concentration des ions Na+
Le dosage des ions Na+ n'est pas réalisable par des méthodes colorimétriques simples. Leur concentration de ces ions ne sera donc pas déterminée directement. Toutefois, on peut en obtenir une estimation approximative en établissant un bilan des ions positifs et négatifs présents dans l'eau.
L'analyse permet en effet de mesurer la plus grande partie des ions négatifs (HCO3-, NO3-, Cl-, SO42- ).
b Si les ions Fe3+ ne sont pas présents en quantité importante, on peut considérer que les ions Na+ doivent compléter la somme des ions positifs ( Ca2+, Mg2+, K+ ...).
B.1.7. Les ions ammonium NH4+, les nitrites NO2- et les nitrates NO3-
Ces ions proviennent essentiellement des engrais agricoles et de la minéralisation de l'azote organique abandonné par les êtres vivants. La moitié des engrais simples azotés consommés par l'agriculture se trouve sous forme d'ammonitrates : les ions ammonium se fixent partiellement dans le sol, mais les nitrates très solubles migrent vers les nappes et les rivières s'ils ne sont pas absorbés par les plantes.
Les eaux souterraines peuvent contenir de faibles quantités d'ions ammonium, généralement inférieures à 1 mg/l. Dans des eaux d'égout, ces ions sont libérés par la dégradation des protéines et de l'urée. La présence de concentrations élevées dans un cours d'eau indique une zone de pollution organique ou d'eutrophisation.
Les nitrites peuvent être présents dans les nappes aquifères suite à la dénitrification anaérobie. Dans les rivières, ils proviennent de l'oxydation de l'ammonium par des bactéries et leur concentration reste très faible.
Les poissons seraient incapables d'éliminer les nitrites : ceux-ci sont mortels pour la truite à des doses inférieures au microgramme par litre.Les nitrates qui se rencontrent dans les rivières et les eaux souterraines ont une origine essentiellement agricole (engrais, élevages industriels...) et urbaine (égouts). Les concentrations en nitrates des eaux souterraines sont en augmentation dans beaucoup de régions et certaines réserves souterraines risquent de devenir inconsommables. Il faut entre 6 et 15 ans pour que les nitrates répandus en excès sur les cultures se retrouvent dans les nappes aquifères.
Les nitrates contenus dans les cours d'eau sont consommés par la végétation, mais des concentrations trop élevées favorisent une croissance exagérée des algues et des plantes aquatiques et provoquent avec les phosphates une eutrophisation.
Les normes CEE sont strictes pour les eaux de boisson qui doivent contenir moins de 50 mg de nitrate par litre. La norme conseillée pour les nourrissons est encore plus faible car leur estomac, moins acide que celui des adultes, contient des bactéries qui transforment les nitrates en nitrites et peuvent provoquer une méthémoglobinémie (les nitrites transforment l'hémoglobine du sang en méthémoglobine incapable de fixer l'oxygène).
![]() Dosage de l'ammonium avec le réflectomètre Merck.
Dosage de l'ammonium avec le réflectomètre Merck.
Mode opératoire
1. Suivre les instructions du réflectomètre RQflex.
2. Pour le Test Ammonium :
3. Procédure A
4. Temps de réaction mémorisé : 480 secondes.
5. Rincer plusieurs fois le tube à essai avec l'échantillon préparé (20 - 30 °C), puis le remplir jusqu'au repère de 5 ml.
6. Ajouter 10 gouttes de réactif NH4 - 1 et agiter.
7. Ajouter 1 microcuiller bleue arasée (fixée dans le bouchon du flacon NH4 - 2) de réactif NH4 - 2 et dissoudre en agitant.
8. Prélever 1 bandelette et reboucher immédiatement le tube.
9. Presser la touche START du réflectomètre et absolument en même temps placer pendant 8 minutes la bandelette analytique dans la solution à mesurer de telle manière que les deux zones réactionnelles soient entièrement humectées.
10. 10 secondes avant la fin de la réaction, retirer la bandelette de la solution et la secouer vigoureusement pour en éliminer l'excédent de liquide. Puis introduire immédiatement la bandelette dans le compartiment de lecture jusqu'à la butée, les zones réactionnelles étant tournées vers l'affichage.
11. Lire sur l'affichage le résultat d'analyse en mg/l de NH4+
12. Le résultat est mémorisé automatiquement.Dosage des nitrites avec le réflectomètre Merck.
Mode opératoire
1. Suivre les instructions du réflectomètre RQflex.
2. Pour le test Nitrites :
3. Procédure A. Temps de réaction mémorisé : 15 secondes.
4. Prélever 1 bandelette et reboucher immédiatement le tube.
5. Presser la touche START du réflectomètre et, en même temps plonger les deux zones réactionnelles de la bandelette pendant environ 2 secondes dans la solution à analyser (15 - 30°C).
6. Secouer la bandelette pour en éliminer l'excédent de liquide.
7. Dés que le bip sonore se déclenche (5 secondes avant la fin de la réaction), introduire la bandelette dans le compartiment de lecture jusqu'à la butée, les zones réactionnelles étant tournées vers l'affichage.
8. Lire le résultat d'analyse sur l'affichage. Le résultat est mémorisé automatiquement.
![]() Dosage des nitrates avec le réflectomètre Merck.
Dosage des nitrates avec le réflectomètre Merck.
Mode opératoire.
1. Suivre les instructions du reflectomètre RQflex. Pour le Test Nitrates : Procédure A. Temps de réaction mémorisé : 60 secondes.
2. Prélever 1 bandelette analytique et reboucher immédiatement le tube.
3. Presser la touche START du réflectomètre et, absolument en même temps, plonger les deux zones réactionnelles de la bandelette pendant environ 2 secondes dans l'échantillon préparé (15-30°C).
4. Secouer vigoureusement la bandelette pour en éliminer l'exédent de liquide.
5. Dès que le bip sonore se déclenche (5 secondes avant la fin de la réaction), introduire la bandelette dans le compartiment de lecture jusqu'à la butée, les zones réactionnelles étant tournées vers l'affichage.
6. Lire sur l'affichage le résultat d'analyse en mg/l de NO3-. Le résultat est mémorisé automatiquement.